I. Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hóa học
1. Phản ứng một chiều
– Phản ứng chỉ ra theo một chiều từ trái sang phải được gọi là phản ứng một chiều.
– Chất phản ứng biến đổi hoàn toàn thành chất sản phẩm và không xảy ra theo chiều ngược lại.
2. Phản ứng thuận nghịch
– Phản ứng hóa học trong đó chất phản ứng biến đổi thành chất sản phẩm và đông thời chất sản phẩm lại phản ứng với nhau để biến thành chất tham gia phản ứng. Những phản ứng này gọi là phản ứng thuận nghịch.
Ví dụ:
Cl2 + H2O (rightleftharpoons) HCl + HClO
– Chiều mũi tên từ trái sang phải là chiều phản ứng thuận.
– Chiều mũi tên từ phải sang trái là chiều phản ứng nghịch.
3. Cân bằng hóa học
– Là trạng thái của phản ứng thuận nghịch, ở đó trong cùng một đơn vị thời gian có bao nhiêu phân tử chất sản phẩm được hình thành từ những chất ban đầu thì có bấy nhiêu phân tử chất sản phẩm phản ứng với nhau để tạo thành chất ban đầu.
=> Trạng thái này của phản ứng thuận nghịch được gọi là cân bằng hóa học.
– Cân bằng hóa học là trạng thái của phản ứng thuận nghịch khi tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
II. HẰNG SỐ CÂN BẰNG HÓA HỌC
1. Cân bằng trong hệ đồng thể
– Hệ đồng thể là hệ mà các tính chất lí học và hóa học đều như nhau ở mọi vị trí trong hệ.
Thí dụ: hệ gồm các chất khí, hệ gồm các chất tan trong dung dịch.
– Giả sử có một phản ứng thuận nghịch sau:
aA + bB (rightleftharpoons) cC + dD
A, B, C, D là những chất khí hoặc những chất tan trong dung dịch phản ứng ở trạng thái cân bằng, ta có:
K = (frac{[C]^{c}[D]^{d}}{[A]^{a}[B]^{b}})
– Trong đó: [A], [B], [C], [D] là nồng độ mol/l của các chất A, B, C và D; a, b, c, d là hệ số các chất trong phương trình phản ứng.
– Hằng số cân bằng K của phản ứng xác định chỉ phụ thuộc vào nhiệt độ, không phụ thuộc vào nồng độ chất phản ứng.
– Trường hợp cân bằng được thiết lập giữa các chất khí, người ta có thể thay nồng độ các chất trong biểu thức tính K bằng áp suất riêng phần của hỗn hợp.
2. Cân bằng trong hệ dị thể
– Hệ dị thể là hệ mà các tính chất lí học hóa học là không giống nhau ở mọi vị trí trong hệ. Thí dụ: hệ gồm chất rắn và chất khí; hệ gồm chất rắn và chất tan trong nước.
– Xét hệ cân bằng sau:
C(r) + CO2 (k) (rightleftharpoons) 2CO (k)
K = (frac{[CO]^{2}}{[CO_{2}]}) Nồng độ các chất rắn được coi là hằng số.
III. SỰ CHUYỂN DỊCH CÂN BẰNG HÓA HỌC
1. Định nghĩa
Sự chuyển dịch cân bằng hóa học là sự phá vỡ trạng thái cân bằng cũ để chuyển sang một trạng thái cân bằng mới do các yếu tố bên ngoài tác động lên cân bằng.
2. Các yếu tố ảnh hưởng đến cân bằng hóa học
– Các yếu tố nồng độ, áp suất và nhiệt đọ ảnh hưởng đến cân bằng hóa học đã đc nhà hóa học Pháp Le Chatrlier tổng kết thành nguyên kí được gọi là nguyên lí Le Chatrlier như sau:
– Một phản ứng thuận nghịch đang ở trạng thái cân bằng khi chịu một tác động bên ngoài, như biến đổi nồng độ, áp suất, nhiệt độ, sẽ chuyển dịch cân bằng theo chiều làm giảm tác động bên ngoài đó.
Lưu ý: khi phản ứng ở trạng thái cân bằng, nếu số mol khí ở 2 vế của phương trình bằng nhau thì khi tăng áp suất cân bằng sẽ không chuyển địch.
3. Vai trò chất xúc tác
– Chất xúc tác không làm biến đổi nồng độ các chất trong cân bằng và không làm biến đổi hằng số cân bằng nên không làm cân bằng chuyển dịch.
IV. Ý NGHĨA CỦA TỐC ĐỘ PHẢN ỨNG VÀ CÂN BẰNG HÓA HỌC TRONG SẢN XUẤT HÓA HỌC
– Dựa vào những yếu tố ảnh hưởng đến tốc độ phản ứng hóa học và cân bằng hóa học để chọn lọc nâng cao hiệu suất trong sản xuất hóa học.
Thí dụ: trong sản xuất H2SO4 phải dùng trục tiếp phản ứng:
2SO2 (k) + O2 (k) (rightleftharpoons) 2SO3 ∆H = -198kJ < 0.
– Phản ứng tỏa nhiệt, nên khi tăng nhiệt độ cân bằng chuyển theo chiều nghịch giảm hiệu suất phản ứng. Để cân bằng chuyển dịch theo chiều thuân người ta tăng nồng độ oxi (dùng lượng dư không khí).
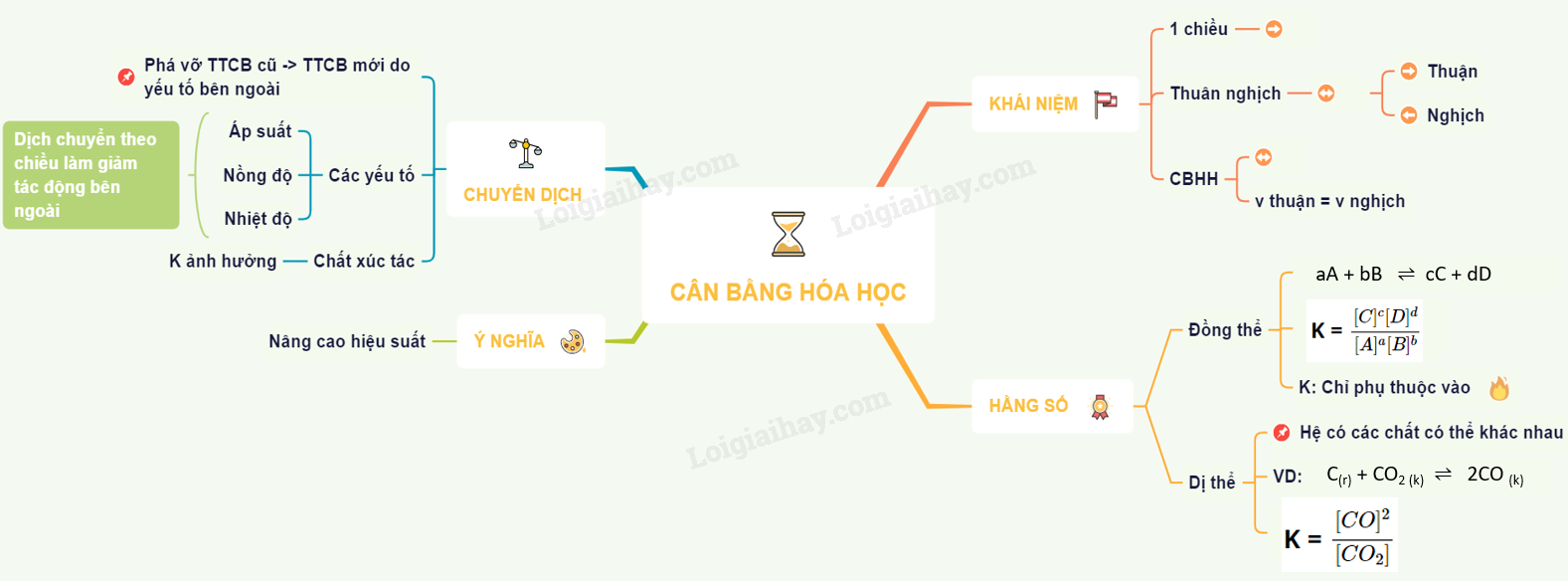
Sơ đồ tư duy: Cân bằng hóa học
Loigiaihay.com